|
亂奣棯亃
偑傫偑戝偒偔側傞偨傔偵偼丄塰梴傗巁慺傪塣傇寣娗傪憹傗偟偰偄偔昁梫偑偁傝傑偡丅怴偟偄寣娗偑憹惗偡傞偙偲傪乽寣娗怴惗乿偲屇傃丄偑傫慻怐偺寣娗怴惗傪慾奞偡傞偙偲偼丄偑傫嵶朎傪暫椘峌傔偵偟偰丄偮偄偵偼偑傫嵶朎偺夠傪彫偝偔偡傞偙偲偑偱偒傑偡丅
偑傫帯椕栻偲偟偰悢懡偔偺寣娗怴惗慾奞嵻偑奐敪偝傟偰偄傑偡偑丄寬峃怘昳偺拞偱寣娗怴惗慾奞惉暘偑娷傑傟傞傕偺偲偟偰乽僒儊擃崪乿偑偁傝傑偡丅弶婜偺偙傠偺尋媶偱偼丄偑傫偺捠忢椕朄偱岠壥偺側偐偭偨枛婜偑傫姵幰傪懳徾偵桳岠惈偑曬崘偝傟丄偑傫帯椕屻偺嵞敪傪梊杊偡傞岠壥傕婜懸偝傟偰偄傑偟偨丅
偟偐偟丄偦偺屻偺戝婯柾側僾儔僙儃懳徠斾妑椪彴帋尡偱偼丄桳岠惈偑斲掕偝傟偰偄傑偡丅
僒儊擃崪暡枛偵娭偟偰偼丄寣娗怴惗慾奞嶌梡傪婜懸偱偒傞検乮侾擔50乣100g乯傪暈梡偡傞偙偲偼崲擄乮摿桳側廘偄傗堓挵忈奞偵傛傞揻偒婥傗怘梸晄怳側偳偺暃嶌梡偑嫮偄乯偲偄偆偙偲偱丄桳梡惈偼斲掕偝傟偰偄傑偡乮岠壥傛傝傕暃嶌梡偺曽偑嫮偄乯丅僒儊擃崪偵娷傑傟傞寣娗怴惗慾奞惉暘傪拪弌偟偨惢昳偑擇廳栍専帋尡偱専摙偝傟偰偄傑偡偑丄尰帪揰偱偼傑偩偑傫帯椕偵偍偗傞桳岠惈偼摼傜傟偰偄傑偣傫丅
偟偨偑偭偰尰帪揰偱偼丄僒儊擃崪傪巊梡偟偨僒僾儕儊儞僩偺偑傫帯椕偵偍偗傞桳岠惈傪帵偡僄價僨儞僗乮徹嫆乯偼柍偄偲偄偆寢榑偵側傝傑偡丅
亂偑傫慻怐偑戝偒偔側傞偵偼寣娗偺怴惗偑昁梫亃
懱偺慻怐偑惗偒偰偄偔偨傔偵偼寣塼偐傜塰梴傗巁慺偺嫙媼傪偆偗傞偙偲偑昁梫偱丄寣娗偑媗傑偭偰寣塼偑棳傟側偔側傞偲慻怐偼巰傫偱偟傑偄傑偡丅偑傫嵶朎偼惓忢嵶朎傪墴偟偺偗偰帺暘彑庤偵憹怋偡傞傛偆偵側偭偨嵶朎偱偡偐傜丄夞傝偺惓忢側慻怐偐傜塰梴傗巁慺傪扗偍偆偲偟傑偡丅偦偺庤抜偲偟偰丄偑傫嵶朎帺恎偑寣娗傪嶌傞抈敀幙乮寣娗憹怋場巕乯傪暘斿偟偰怴偟偄寣娗傪憹傗偦偆偲偟傑偡丅怴偟偄寣娗傪嶌傞偙偲傪寣娗怴惗偲偄偄丄怴惗偟偨寣娗傪宱楬偲偟偰偑傫嵶朎偑揮堏傪婲偙偡応崌傕懡偔側傝傑偡丅
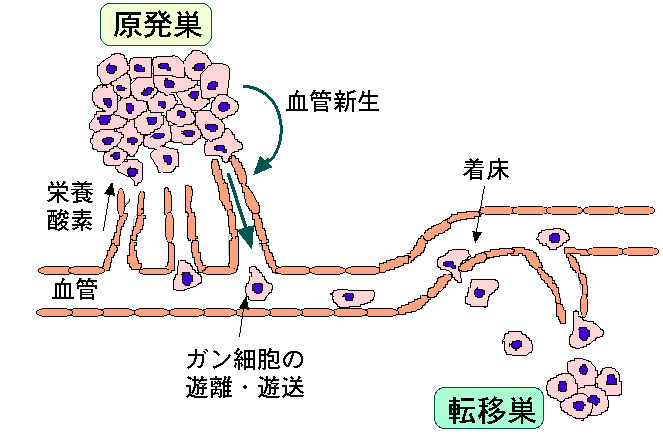
恾丗偑傫嵶朎偼怴惗寣娗傪嶌傝弌偡憹怋場巕傪曻弌偟丄塰梴偲巁慺傪塣傇寣娗傪憹傗偟偰憹怋偡傞丅尨敪憙偐傜梀棧偟偨偑傫嵶朎偼怴惗寣娗傪夘偟偰寣娗撪偵擖偭偰懠偺応強偵塣偽傟乮梀憲乯丄寣娗暻偵拝彴偟丄寣娗奜偵弌偰揮堏憙傪宍惉偡傞丅
亂僒儊擃崪偐傜怴惗寣娗梷惂暔幙偑尒偮偐偭偰偄傞亃
偑傫慻怐偺寣娗怴惗傪梷偊傞偙偲偑偱偒傟偽丄偑傫偺憹怋傗揮堏傪巭傔傞偙偲偑偱偒丄偑傫嵶朎偑塰梴傗巁慺傪庢傝崬傔側偔側傞偲偑傫嵶朎偼巰偵偄偨傝傑偡丅偦偙偱丄寣娗怴惗傪梷偊傞栻偑峈偑傫嵻偲偟偰奐敪偝傟傞傛偆偵側傝傑偟偨丅寬峃怘昳偱偼僒儊偺擃崪偑偑傫慻怐偺寣娗怴惗傪梷偊傞傕偺偲偟偰拲栚偝傟傑偟偨丅
僒儊擃崪偺惉暘偺拞偵寣娗怴惗慾奞暔幙偑尒偮偐傝丄偑傫傗墛徢惈幘姵偺寣娗怴惗傪梷偊傞栚揑偱奐敪偝傟傑偟偨丅僒儊擃崪僄僉僗偺奐敪幰偱偁傞儗乕儞攷巑偺惢朄偼摿嫋偑擣壜偝傟丄暡枛僒儊擃崪僄僉僗偺僇乕僥傿儗僀僪偼93擭12寧丄暷崙怘昳堛栻昳嬊傛傝偑傫偺帯尡栻偲偟偰彸擣傪庴偗偰偄傑偡丅 弶婜偺崰偺尋媶偱偼丄僒儊擃崪惢嵻偺寣娗怴惗慾奞嶌梡偑恖娫偱傕娤嶡偝傟丄摦暔幚尡側偳偱峈庮釃岠壥偑曬崘偝傟偰偄傑偡丅偟偐偟丄僾儔僙儃懳徠椪彴帋尡偱偼丄尰帪揰偱偼傑偩桳岠惈偼妋擣偝傟偰偄傑偣傫丅乮暥專嶲徠乯
亂暥專揑峫嶡亃
仜僒儊擃崪偺峈庮釃岠壥偵偼巀斲偑偁傞丅
Oral shark cartilage does not abolish carcinogenesis but delays tumor progression in a murine model.乮儅僂僗偺幚尡儌僨儖偱僒儊擃崪偺宱岥愛庢偼敪偑傫傪梷惂偟側偐偭偨偑丄庮釃偺恑揥傪抶傜偣傞乯Anticancer Res 21:1065-9, 2001擭
儅僂僗偵敪偑傫嵻傪搳梌偟偰敪惗偝偣傞恡憻偑傫偺幚尡儌僨儖偱丄暡枛壔偟偨僒儊擃崪傪宱岥搳梌偡傞偲丄恡憻偑傫偺敪惗偼僐儞僩儘乕儖孮乮僒儊擃崪旕搳梌乯偱19儢寧偱偁偭偨偺偵懳偟偰丄僒儊擃崪搳梌孮偱偼55儢寧偱偁偭偨丅僒儊擃崪偵偼儅僂僗偺恡憻敪偑傫儌僨儖偵偍偄偰丄偑傫壔偺恑揥懍搙傪抶傜偣傞岠壥偑偁偭偨丅
|
The effect of shark cartilage extracts on the growth and metastatic spread of the SCCVII carcinoma.乮SCCVII偑傫嵶朎偺憹怋偲揮堏偵懳偡傞僒儊擃崪偺岠壥乯Acta Oncol 37:441-5, 1998擭
儅僂僗偵SCCVII 偲偄偆偑傫嵶朎傪堏怉偟偨幚尡偱丄僒儊擃崪暡枛傪宱岥搳梌偟偰傕丄偑傫慻怐偺憹戝懍搙傗揮堏傪梷惂偡傞岠壥偼擣傔側偐偭偨丅
|
| 1997擭偺抜奒偱偼僒儊擃崪僄僉僗偺峈庮釃岠壥偼妋擣偝傟偰偄側偄丅暷崙偺偑傫帯椕尋媶嵿抍偑娻姵幰傪懳徾偵戝婯柾尋媶傪峴偄丄恑峴偑傫姵幰偵戝検偺僒儊偺擃崪偺暡枛傪愛庢偝偣丄峈偑傫嶌梡偑偁傞偐偳偆偐尋媶偟偨丅偟偐偟丄峈偑傫嶌梡偼妋擣偱偒側偐偭偨偲丄戞33夞暷崙椪彴庮釃妛夛偱曬崘偝傟偨丅乮Medical Tribune 1997擭8寧21擔乯 |
仜寣娗怴惗慾奞嶌梡偺壜擻惈偼曬崘偝傟偰偄傞丅
Demonstration of inhibitory effect of oral shark cartilage on basic fibroblast growth factor-induced angiogenesis in the rabbit cornea.乮僂僒僊偺妏枌偵偍偗傞墫婎惈慄堐夎嵶朎憹怋場巕桿摫惈偺寣娗怴惗偵懳偡傞宱岥僒儊擃崪偺慾奞岠壥乯Biol Pharm Bull 24:151-4, 2001擭
墫婎惈慄堐夎嵶朎憹怋場巕乮bFGF乯傪娷傫偩儁儗僢僩傪僂僒僊偺妏枌偵堏怉偟偰丄寣娗怴惗傪巋寖偡傞幚尡儌僨儖偵偍偄偰丄暡枛壔偟偨僒儊擃崪偺宱岥搳梌偼丄bFGF偱堷偒婲偙偝傟傞寣娗怴惗傪慾奞偟偨丅偮傑傝丄暡枛壔偟偨僒儊擃崪傪岥偐傜愛庢偟偰傕丄妏枌偵偍偗傞寣娗偺怴惗傪梷偊傞儗儀儖偺慾奞暔幙偑媧廂偝傟傞丅 |
仜恖偵偍偗傞寣娗怴惗偵懳偡傞慾奞岠壥傕巜揈偝傟偰偄傞丅
Antiangiogenic effects of the oral administration of liquid cartilage extract in humans.乮僸僩偵偍偗傞塼懱僒儊擃崪僄僉僗偺宱岥愛庢偺寣娗怴惗慾奞嶌梡乯J Surg Res 87:108-13, 1999擭
儌儞僩儕僆乕儖堛壢戝妛偺僸僩偺儃儔儞僥傿傾偱偺尋媶丅29恖偺寬峃側抝惈儃儔儞僥傿傾傪儔儞僟儉偵俁孮偵暘偗丄塼懱僒儊擃崪僄僉僗傪23擔娫枅擔宱岥搳梌偟丄12擔栚偵億儕價僯乕儖傾儖僐乕儖傪媗傔偨寠偺偁偄偨僔儕僐儞僠儏乕僽傪慜榬晹偺旂壓偵杽傔崬傫偩丅23擔栚偵僠儏乕僽傪庢傝彍偒丄撪旂嵶朎偺枾搙側偳偱寣娗怴惗偺掱搙傪慻怐妛揑偵斾妑偟偨丅塼懱僒儊擃崪傪侾擔検偱侽倣倢丄俈倣倢丄21倣倢丄搳梌偟偨僌儖乕僾偺寣娗撪旂嵶朎枾搙偼偦傟偧傟丄 3.15 +/- 0.11 丄2.24 +/- 0.10丄2.47 +/- 0.10偱偁偭偨丅寢崌慻怐偺検偺巜昗偱偁傞僸僪儘僉僔僾儘儕儞偺検偵偼嵎偼擣傔側偐偭偨丅偙傟傜偺寢壥傛傝丄塼懱僒儊擃崪偺暈梡偑憂彎偵偍偗傞寣娗怴惗傪慾奞偡傞椪彴岠壥偑偁傞偙偲偑帵嵈偝傟偨丅 |
仜僒儊擃崪拞偺寣娗怴惗慾奞暔幙偲偟偰僾儘僥僆僌儕僇儞傗儁僾僠僪側偳偑巜揈偝傟偰偄傞丅
The characterization of angiogenesis inhibitor from shark cartilage.乮僒儊擃崪偵娷傑傟傞寣娗怴惗慾奞暔幙偺惈忬乯Adv Exp Med Biol 476:209-23, 2000擭
僒儊擃崪偐傜拪弌偝傟偨寣娗怴惗慾奞場巕偺SCF2偺夝愅傪曬崘丅SCF2偼暘巕検偑栺10僉儘僟儖僩儞偺丄働儔僞儞棸巁偲儁僾僠僪僌儕僇儞傪娷桳偡傞懴擬惈偺僾儕僥僆僌儕僇儞偱偁偭偨丅
|
Effect of U-995, a potent shark cartilage-derived angiogenesis inhibitor, on anti-angiogenesis and anti-tumor activities.乮僒儊擃崪桼棃寣娗怴惗慾奞暔幙U-995偺寣娗怴惗慾奞嶌梡偲峈庮釃岠壥乯Anticancer Res 18:4435-41, 1998擭
僒儊擃崪偐傜拪弌偝傟偨寣娗怴惗慾奞暔幙偱偁傞U-995偼丄暘巕検偑10僉儘僟儖僩儞偲14僉儘僟儖僩儞偺俀偮偺儁僾僠僪偐傜峔惉偝傟偰偄偨丅U-995偼寣娗撪旂嵶朎偺憹怋傪梷惂偟丄僐儔乕僎儞偺梟夝傪慾奞偟丄寣娗怴惗偲偑傫嵶朎偺憹怋傪梷惂偟偨丅 |
Angiogenic inhibitor protein fractions derived from shark cartilage.乮僒儊擃崪桼棃偺寣娗怴惗慾奞抈敀乯Biosci Rep 28:15-21, 2008
僒儊擃崪拞偺寣娗怴惗慾奞暔幙偲偟偰暘巕検 14.7 偲 16 kDa偺抈敀幙傪摨掕偟偨丅 |
仜恑峴攛偑傫傪懳徠偲偟偨僾儔僙儃懳徠擇廳栍専帋尡偱偼丄峈庮釃岠壥偼擣傔傜傟側偐偭偨丅
Chemoradiotherapy with or without AE-941 in stage III non-small cell lung cancer: a randomized phase III trial.乮僗僥乕僕III偺旕彫嵶朎惈攛偑傫偵懳偡傞壔妛曻幩慄椕朄偲AE-941偺岠壥丗儔儞僟儉壔戞俁憡椪彴帋尡乯J Natl Cancer Inst. 102(12):859-65. 2010
寣娗怴惗慾奞嵻偑旕彫嵶朎惈攛偑傫傗偦偺懠偺偑傫偺姵幰偺惗懚婜娫傪墑挿偝偣傞岠壥偑曬崘偝傟偰偄傞丅塼懱僒儊擃崪僄僉僗偵偼寣娗怴惗慾奞嶌梡偑偁傞偙偲偑曬崘偝傟偰偄傞偨傔丄峈偑傫嶌梡偑婜懸偝傟偰偄傞丅偦偙偱丄庤弍晄擻偺僗僥乕僕III偺旕彫嵶朎惈攛偑傫姵幰傪懳徾偲偟偨戞俁憡椪彴帋尡乮暷崙偲僇僫僟偺嫟摨尋媶偵傛傞儔儞僟儉壔僾儔僙儃懳徠擇廳栍尡帋尡乯偵偰丄昗弨壔偝傟偨僒儊擃崪惢嵻AE-941偺岠壥傪専摙偟偨丅
庤弍晄擻偺僗僥乕僕III偺旕彫嵶朎惈攛偑傫姵幰379恖傪懳徾偵丄捠忢偺壔妛曻幩慄帯椕傪峴偄丄AE-941搳梌傪暪梡偟偨孮偲僾儔僙儃乮婾栻乯傪搳梌偟偨孮偵暘偗偰斾妑専摙偟偨丅偦偺寢壥丄慡懱偺惗懚婜娫丄柍恑峴惗懚婜娫丄憈岟棪側偳慡偰偺巜昗偵偍偄偰丄AE-941搳梌孮偼僾儔僙儃孮偲桳堄嵎傪擣傔側偐偭偨丅
暯嬒惗懚婜娫偼僾儔僙儃孮偑15.6儢寧偵懳偟偰AE-941搳梌孮偼14.4儢寧偱偁偭偨丅柍恑峴惗懚婜娫乮progression-free survival乯偼丄僾儔僙儃孮偑10.7儢寧偵懳偟偰AE-941搳梌孮偼11.3儢寧偱丄摑寁揑偵嵎偼擣傔側偐偭偨丅暃嶌梡偺掱搙偵傕椉幰娫偵嵎傪擣傔側偐偭偨丅偡側傢偪丄庤弍晄擻偺僗僥乕僕III偺旕彫嵶朎惈攛偑傫姵幰偺壔妛曻幩慄帯椕偵僒儊擃崪僄僉僗偺AE-941傪暪梡偟偰傕丄桳梡惈偼擣傔傜傟側偐偭偨丅
|
埲忋傪傑偲傔傞偲
侾乯僒儊擃崪偺暡枛偦偺傕偺傪惢昳壔偟偨僒僾儕儊儞僩偵偼丄偑傫帯椕偵偍偗傞桳岠惈傗桳梡惈偼擣傔傜傟側偄丅乮僒儊擃崪暡枛偺夁忚愛庢偵傛偭偰崅僇儖僔僂儉寣徢偺暃嶌梡偑敪惗偡傞壜擻惈偑巜揈偝傟偰偄傞乯
俀乯僒儊擃崪拞偵娷傑傟傞寣娗怴惗慾奞暔幙側偳偺峈庮釃惉暘傪拪弌丒擹弅偟偨惢昳偵娭偟偰偼丄偁傞掱搙偺桳岠惈傪帵嵈偡傞曬崘偼偁傞偑丄尰嵼傑偱乮2010擭俈寧偺帪揰乯偺椪彴帋尡偺寢壥偐傜偼丄僒儊擃崪惢昳傪偑傫帯椕偵巊梡偡傞偙偲傪悇彠偱偒傞僄價僨儞僗偼朢偟偄丅
乮怴偟偄惢昳偺奐敪側偳偱丄桳梡側傕偺偑弌偰棃傞壜擻惈偼巆偝傟偰偄傞偑丄尰帪揰偱偼悇彠偱偒傞惢昳偼柍偄乯
栠傞

恾傪僋儕僢僋偡傞偲僋儕僯僢僋偺僒僀僩偵堏摦偟傑偡丅
|

